Reações orgânicas são as reações que acontecem entre compostos orgânicos. Há vários tipos de reações. As principais reações orgânicas são:
Reação de Adição; Reação de Substituição; Reação de Oxidação; Reação de Eliminação.Desse modo, elas ocorrem mediante a quebra de moléculas dando origem a novas ligações. Muito utilizadas na indústria, é a partir delas que podem ser produzidos medicamentos e produtos de cosmética, plásticos, dentre tantas outras coisas.
Alguns exemplos de reações químicas importantes que envolvem substâncias orgânicas são: combustão dos hidrocarbonetos presentes no gás de cozinha (propano e butano), nos derivados do petróleo; a gasolina e o óleo diesel. Além disso, faz reações em biocombustíveis, no carvão e na madeira.
Sendo assim, nessa matéria iremos mostrar os principais tipos de reações orgânicas e como elas acontecem. Então fique ligado!
Reações Orgânicas
Reação de Adição
As reações orgânicas de adição, acontecem quando as ligações da molécula orgânica se rompem e à ela é adicionado um reagente. Ou seja, a junção de duas ou mais moléculas originam unicamente um produto.
Acontece principalmente em compostos cujas cadeias sejam abertas e que tenham insaturações, como alcenos e alcinos. Desse modo, rompendo a ligação pi (π) e adicionado átomos à molécula em uma ligação simples. Assim como na figura abaixo:
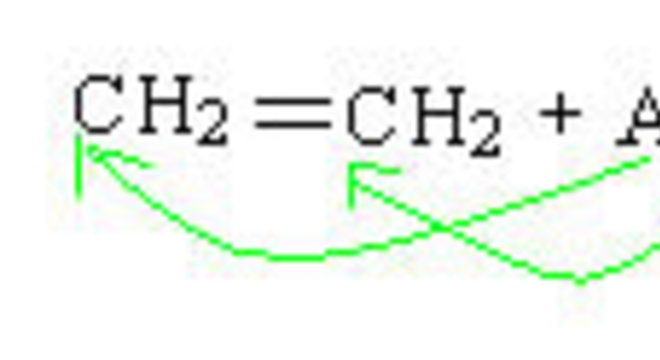
Portanto, veja a seguir exemplos de reações de adição.
Hidrogenação (adição de hidrogênio)As reações orgânicas de hidrogenação ocorrem com gás hidrogênio (H2), catalisada por metal. Portanto, se a reação for de um alceno, produz um alcano, assim como na reação abaixo:
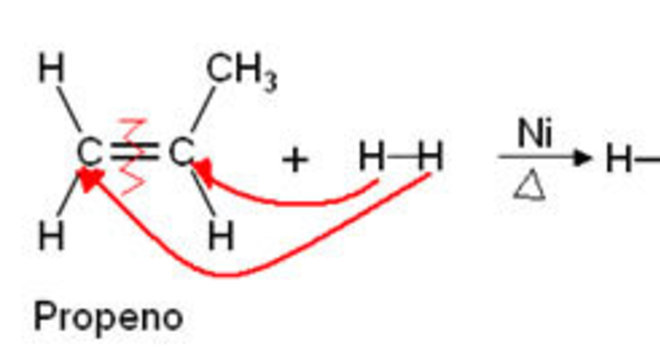
Os halogênios são os elementos da família 17A da Tabela Periódica.
Porém, desses, os mais utilizados são: Cl2 e Br2. Nesse caso, há a formação de um dialeto de alquila, ficando assim:
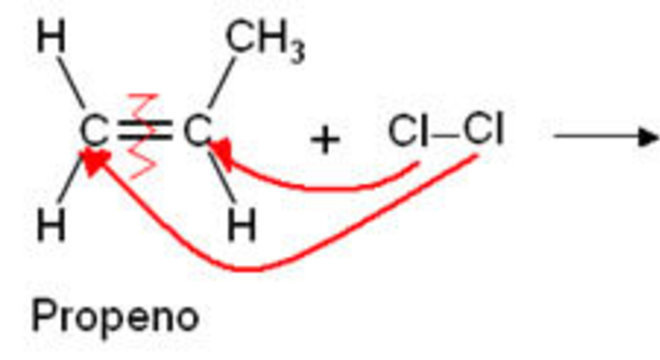
Essas reações orgânicas de hidratação ocorrem em meio ácido como catalisador e há a formação de um álcool.
Com exceção do eteno, os outros alcenos somente originam álcoois secundários segundo essa reação:
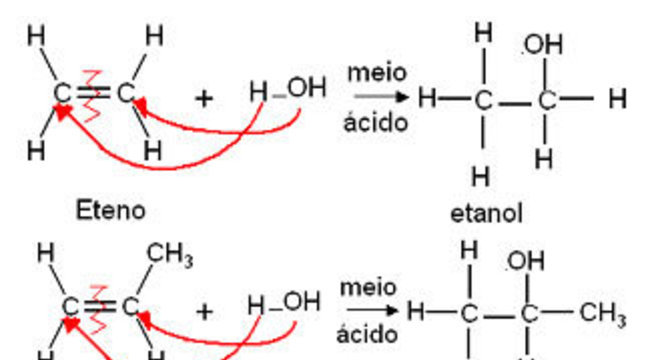
Reação de Substituição
As reações orgânicas de substituição, acontecem quando um átomo ou grupo de átomos é substituído por um radical do outro reagente, ou seja, ocorre na molécula a troca de um ligante.
Portanto, essa situação acontece principalmente entre alcanos, ciclanos e aromáticos. A equação abaixo exemplifica uma reação de substituição, onde R-H representa um alcano:
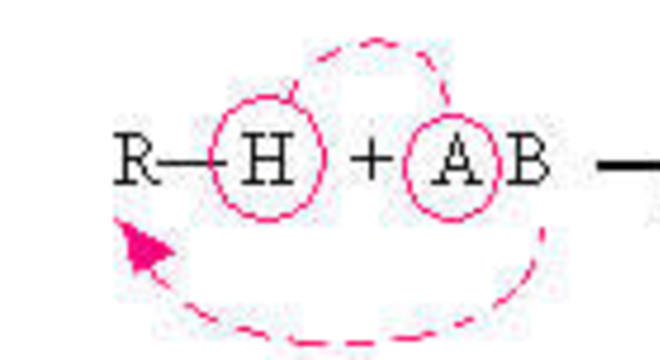
Desse modo, confira a seguir exemplos de reações de substituição.
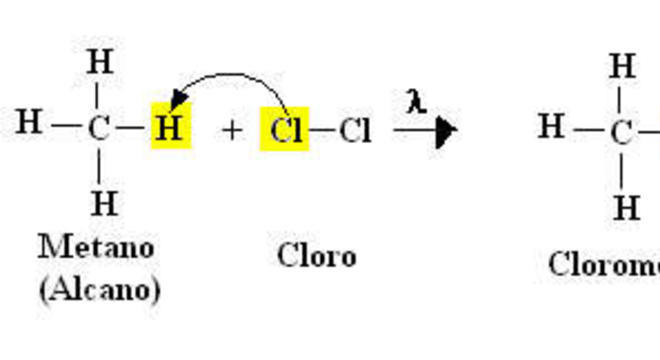
Halogenação (substituição por halogênio)Essas reações orgânicas ocorrem quando uma ou mais moléculas de halogênios reage com o alcano, conforme mostrado abaixo na reação de obtenção do cloreto de metila, ou clorometano:
As reações orgânicas de nitração são as substituições de um ou mais átomos de hidrogênio de um alcano por um ou mais grupos nitro – NO2, em presença de ácido nítrico, concentrado e a quente.
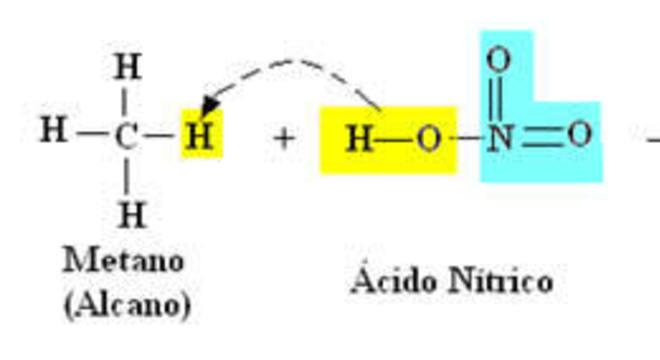
Na reação acima foi formado o nitrometano, que é usado para combustível de automóveis.
Portanto, é possível observar que em toda reação de nitração, são formados nitroalcanos e água.
Sulfonação (substituição por sulfônicos)Essas reações orgânicas correspondem à substituição de um ou mais átomos de hidrogênio de um alcano por um ou mais grupos sulfônicos (-SO3H).
Neste caso, só é possível que o alcano reaja como ácido sulfúrico se ele tiver mais de 6 carbonos, assim como na reação abaixo:
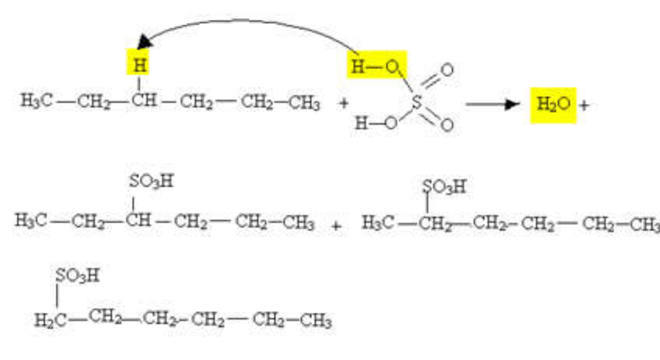
Além disso, existem outros exemplos importantes de reações orgânicas de substituição:
Alquilação: ocorre com os aromáticos e com os haletos orgânicos, em que pelo menos um de seus hidrogênios é substituído por um radical alquila; Acilação: um hidrogênio do anel aromático é substituído por um grupo acila; Hidrólise alcalina: ocorre com os haletos orgânicos quando sofrem quebra na presença de uma solução aquosa de base forte e álcoois são formados como produtos.Reações de Oxidação
As reações orgânicas de oxidação, também chamada de oxirredução, acontece quando há ganho ou perda de elétrons.
Sendo assim, confira a seguir exemplos de reações de oxidação.
Oxidação enérgica dos alcenosEsta oxidação ocorre nos alcenos em contato com um agente oxidante em solução aquosa, concentrada e ácida (geralmente em ácido sulfúrico).
Nesta reação, podemos obter vários produtos, dependendo do tipo da posição da ligação dupla. Observe:
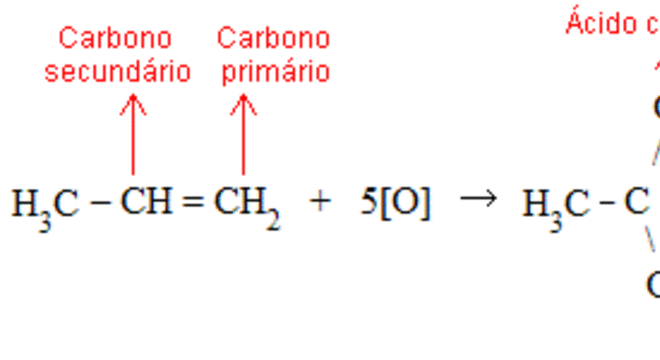
Carbono primário produz gás carbônico e água; Carbono secundário produz ácido carboxílico; Carbono terciário produz cetona.Esta reação serve como teste de insaturação de alceno, ou seja, para identificar que tipo de alceno se tem. Acompanhe o exemplo:
Os álcoois primários se oxidam com oxidantes energéticos, como o permanganato de potássio e dicromato de potássio, em meio sulfúrico.
O produto desta oxidação é aldeído. Sendo assim, com mais quantidade de agente oxidante, obtemos um ácido carboxílico, conforme a reação abaixo:
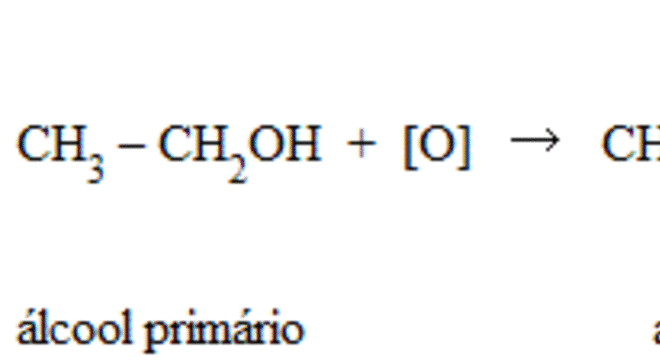
Oxidação de um álcool secundário produz cetona, assim como na reação abaixo:
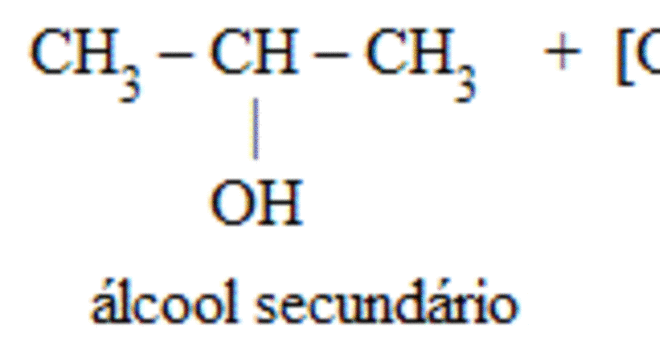
Reação de Eliminação
Por último, outro exemplo de reações orgânicas é a reação de eliminação. Ela acontece quando um ligante de carbono é eliminado da molécula orgânica.
Essa reação é contrária à reação de adição, pois ocorre a saída de ligantes de uma molécula sem que aconteça a substituição desses ligantes por outros.
Sendo assim, existem dois tipos de reação de eliminação:
Eliminação intramolecular: uma molécula elimina alguns de seus átomos; Eliminação intermolecular: duas moléculas interagem, unem-se e eliminam simultaneamente um átomo ou grupo de átomos, sendo, conforme visto anteriormente, o caminho inverso das reações de adição.Desse modo, confira a seguir alguns exemplos de reações de eliminação.
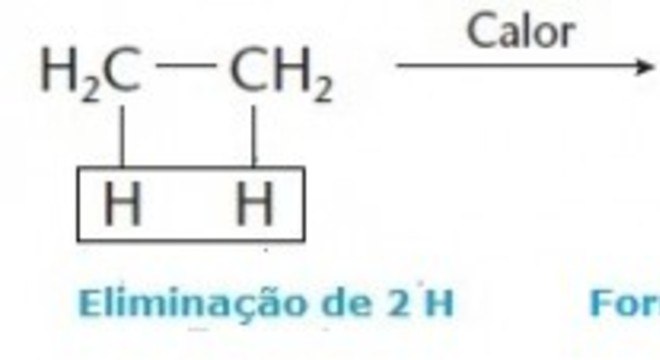
Eliminação de hidrogênio (desidrogenação)Nesse tipo de reação ocorre a eliminação de dois átomos de hidrogênio (H), ao contrário da hidrogenação.
Através da eliminação de hidrogênio é possível converter gorduras saturadas em insaturadas, álcoois em cetonas ou aldeídos (oxidação), alcanos em alcenos e assim por diante.
Sendo assim, observe a demonstração abaixo:
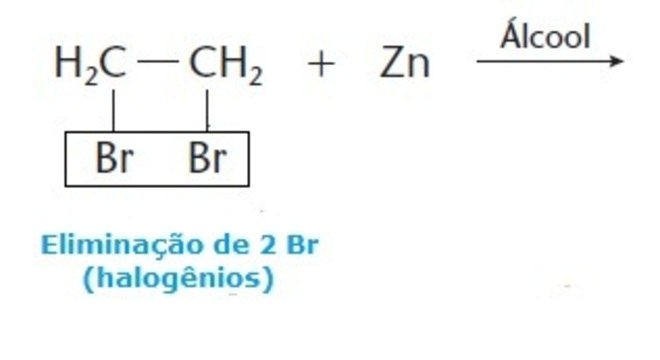
Halogênios são eletronegativos, por isso, sua eliminação é facilitada pela ação de eletropositivos.
Sendo assim, um exemplo de eliminação de halogênios é a reação de brometo de etileno (eletronegativo) com o zinco (eletropositivo), que é catalisada por um álcool e produz um alceno.
As reações orgânicas de halogenidreto seguem a regra de Saytzeff, que diz que carbonos menos hidrogenados tendem a perder hidrogênio com mais facilidade.
Sendo assim, existem duas possibilidades de eliminação:
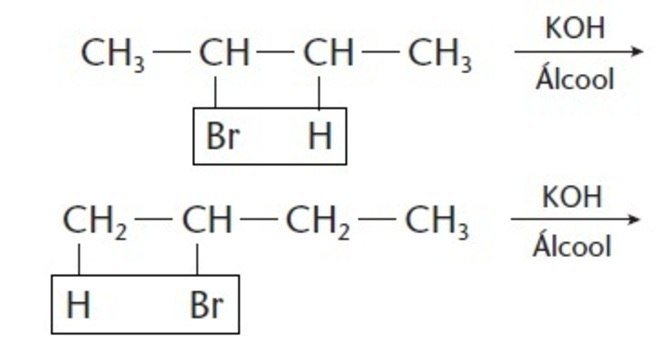
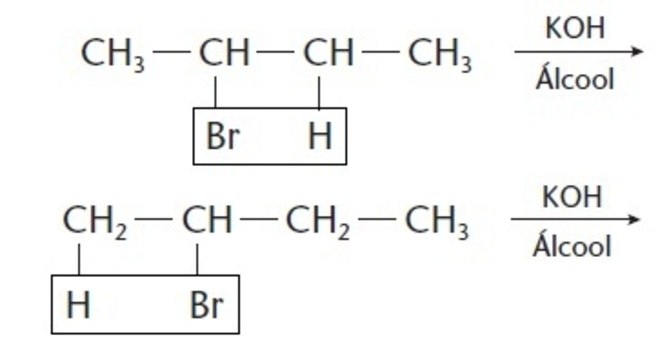
Desse modo, observe que, nestas reações organicas, a eliminação ocorre por meio da ação de hidróxido de potássio (KOH) em solução alcoólica.
O HBr é um ácido e, portanto, é facilmente eliminado da molécula através do KOH, que é uma base.
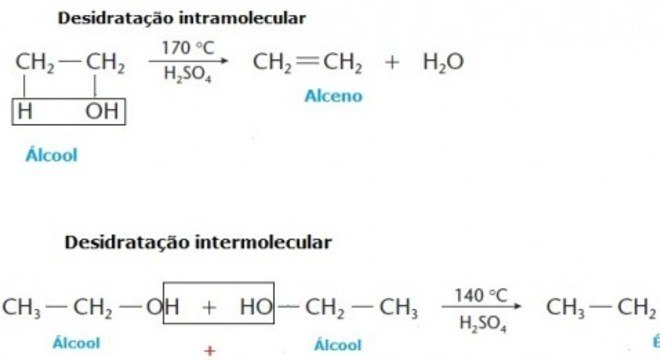
Eliminação de água (desidratação de álcool)As relações orgânicas de desidratação de álcool é caracterizada por ocorrer eliminação de uma ou mais moléculas de água (H2O). Os álcoois, por exemplo, podem sofrer desidratação e esse processo pode ocorrer de duas formas: intramolecular e intermolecular, conforme visto anteriormente.
Sendo assim, álcoois primários tendem a sofrer desidratação intermolecular, produzindo éteres. Contudo, os álcoois secundários e terciários costumam desidrata-se de forma intramolecular, formando seus alcenos correspondentes. Veja os exemplos a seguir:
Portanto, o conhecimento de como essas reações orgânicas se processam é muito importante, principalmente para a síntese orgânica, em que se altera as estruturas das moléculas para a produção de produtos que usamos para diferentes finalidades.
Desse modo, as reações orgânicas são de grande importância para processos industriais, laboratoriais, para o desenvolvimento técnico-cientifico e para o bem-estar da sociedade no geral.
Agora que você conhece os tipos de reações orgânicas e suas finalidades, então está na hora que conhecer várias experiências químicas incríveis para fazer em casa.
Fontes: Toda Matéria, Manual da Química, Brasil Escola
Fonte Imagem Destaque: InfoEnem
Essa matéria Reações Orgânicas – O que são, quais são e suas finalidades foi criada pelo site Conhecimento Científico.